| 일 | 월 | 화 | 수 | 목 | 금 | 토 |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | ||
| 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 13 | 14 | 15 | 16 | 17 | 18 | 19 |
| 20 | 21 | 22 | 23 | 24 | 25 | 26 |
| 27 | 28 | 29 | 30 |
- 노션 필수 단축키
- 노션 블록
- 광계
- 오블완
- 수동수송
- 광호흡
- 차등 전위
- 단백질 분류
- 전주 결혼
- 네른스트 방정식
- 글라이옥시좀
- 역수송체
- 캘빈회로
- 선구동물
- 전주 결혼 준비
- 후구동물
- 인슐린
- 당지질
- 간극연접
- 베타 산화
- 초나선
- 퍼옥시좀
- 신호서열
- 인지질
- 티스토리챌린지
- 노션 단축키
- 밀착연접
- 콜레스테롤
- 인테그린
- 루비스코
- Today
- Total
숭늉의 연구일지
[생물 임용 노트] 단백질 - 3) 단백질의 기능: 단백질과 리간드의 협동적 상호 작용 본문
1. 단백질과 리간드의 협동적 상호작용의 정량적 기술
단백질이 하나가 아닌 여러개(n개)의 리간드와 협동적 상호작용을 할 경우, 이를 정량적으로 기술하면 다음과 같아진다.

위에서 y=ax식으로 표현된 함수의 기울기 n을 nH라고 하며 이를 Hill 계수라고 한다. 이는 단백질과 리간드 결합의 협동성 정도를 나타낸다.

이때 nH의 값에 따라 협동성 정도를 아래와 같이 표현한다.
nH < 1 : 음성 협동
nH > 1 : 양성 협동
nH = n (상한선) : 모두 협동
nH = 1 : 협동성 없음
2. 협동적 상호작용의 예 - Hb(헤모글로빈)
Hb(헤모글로빈) : 적혈구에 존재하는 Heme 보조단 4합체로 구성된 산소 운반 작용에 중요한 역할을 하는 단백질
→ 2개의 Hbα(α1α2), 2개의 Hbβ(β1β2)로 α1β1 - α2β2간의 상호 연결이 있음
Hb는 협동성에 따라 2가지 상태로 구분되는데,
R상태 : 산소의 Hb에 대한 친화도가 높은 상태 - O2 결합이 R상태를 안정화
T상태: deoxyhemoglobin 상태로, O2가 없을 때 안정한 구조
산소가 T상태의 Hb에 결합하면 R상태로 변화가 시작된다.
변화시 소단위 구조의 미미한 변화로 새로운 이온쌍이 형성된다.

Hb는 pO2가 13.3 Kpa인 폐에서 O2와 효과적으로 결합하고, pO2가 4Kpa인 조직에서 O2와 쉽게 해리해야 산소의 전달 과정이 이루어질 수 있다.
→ 산소 결합에 따라 저친화도에서 고친화도로 전환된다. 이는 O2의 한 결합부위의 결합이 다른 분자의 결합 정도에 영향을 미치는 것을 의미한다.
이러한 협동적 리간드 결합에서 그래프는 Sigmoid binding Curve를 보인다.
3. Hb의 산소 운반 영향 요인
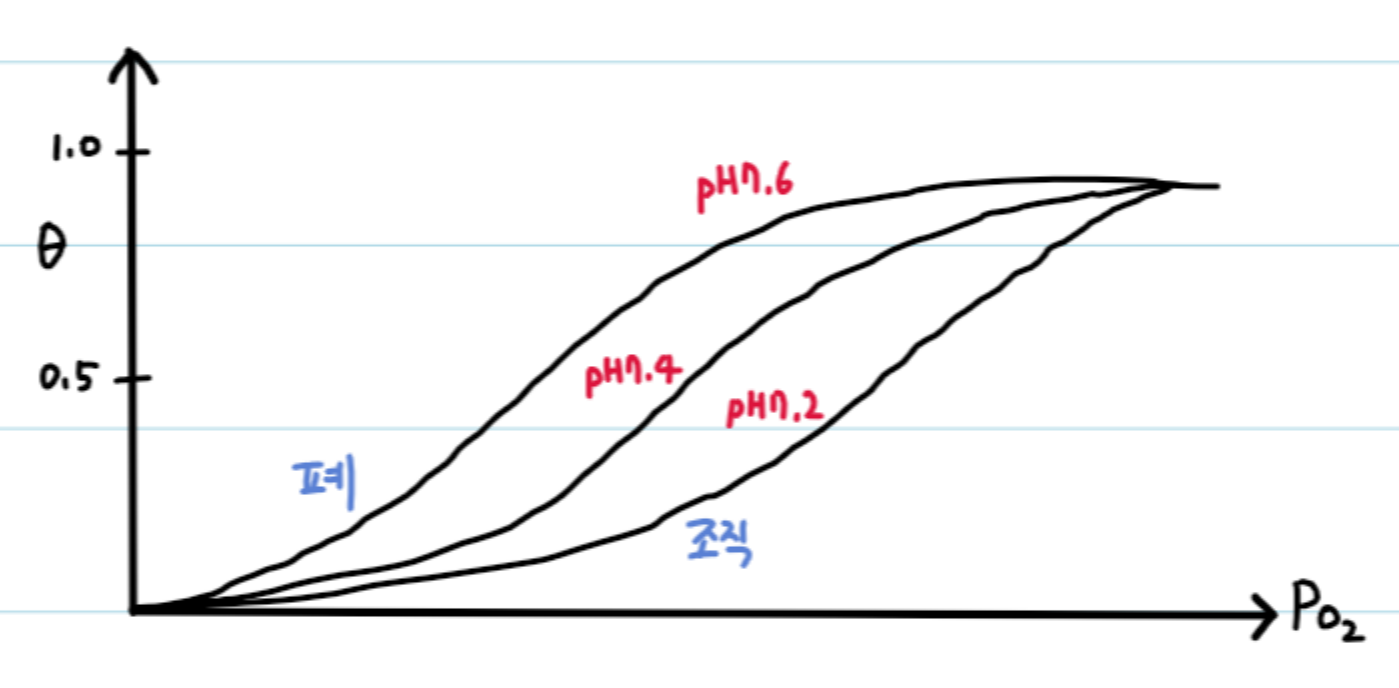
1) 보어 효과
Hb와 같은 산소 운반자가 수용액 또는 혈액 속에 있을 때, CO2 분압이 상승하거나 pH 저하 시 산소 분압 저하 없이도 해리가 촉진된다.
→ Hb에 H+와 CO2가 결합하면 T상태가 안정화된다.
또한 Hb가 CO2와 결합하는 과정에서 방출되는 H+ 또한 보어 효과에 기여한다.
2) BPG(2,3-양인산 글리세르산)
낮은 O2 농도에서 적혈구의 2,3-BPG maltase에 의해 1,3-BPG에서 생성된다(실제 적혈구의 에너지 대사는 해당작용에 의존한다).
낮은 pO2에 대한 생리적 적응으로 고산지대에서 증가하며 Hb의 T상태를 안정화시켜 O2의 친화도를 낮추는 역할을 한다.
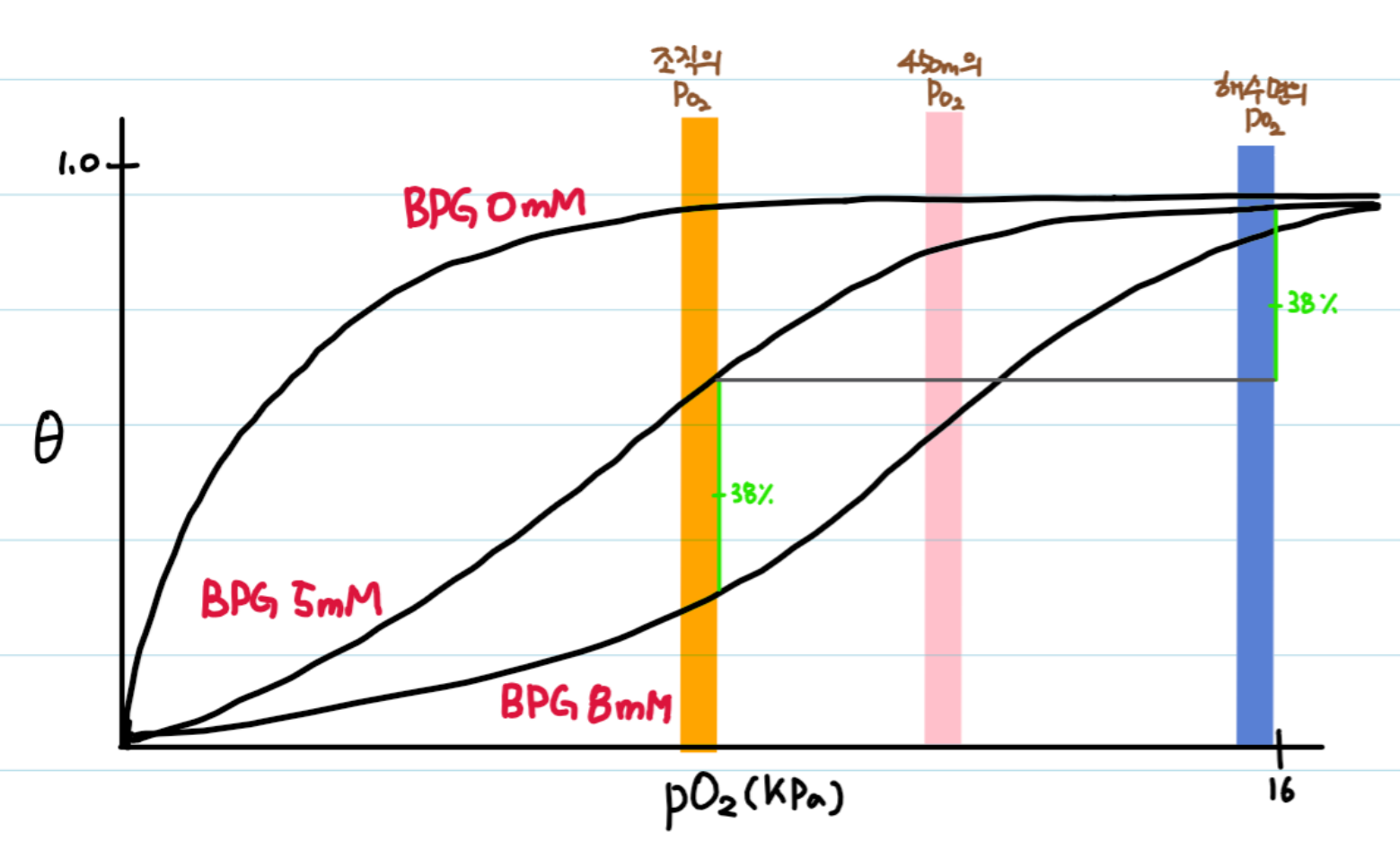
이를 통해 고산지대의 낮은 pO2 상태에서도 해수면에서의 pO2와 비슷한 산소 해리도를 가지게 된다.
4. 입체 다른 자리 효과(allosteric effect)
한 자리에 리간드의 결합이 같은 단백질의 다른 자리 결합 성질에 영향을 주는 것을 말한다.
이러한 역할을 하는 단백질을 조정자라고 하며, 조정자는 그 역할에 따라 억제자(suppressor)와 활성자(activator)로 나뉜다. 만약 리간드가 조정자일 경우 동질 상호작용이라고 하며, 리간드와 조정자가 다른 단백질일 경우 이질 상호작용이라고 한다.
예> Hb의 CO 효과 (여기서 CO는 협동성을 낮추는 억제자 역할을 한다)

5. 항체(antibody)
면역 글로불린(Ig)이라고도 하며, 각 Ig는 4개의 PP(폴리펩타이드)로 이루어져 있다.
이들 폴리펩타이드를 중쇄(heavy chain)와 경쇄(light chain)라고 하며, 항체는 2개의 중쇄와 2개의 경쇄가 Y자 모양으로 결합되어 있다.
항체는 크게 IgA, IgD, IgE, IgG, IgM 5가지로 구분되며 각 항체마다 특징적인 중쇄를 갖는다.

항체 결합의 특이성은 중쇄와 경쇄 끝에 존재하는 가변영역의 아미노산 잔기에 의해 결정된다. 이들 결합의 특이성은 전하, 극성, 비극성, 수소결합 등이 다른 잔기들의 위치와 형태에 의해 부여된다.
'생물학 임용노트 > 단백질' 카테고리의 다른 글
| [생물 임용 노트] 효소 - 2) 효소의 촉매 작용 (0) | 2023.01.03 |
|---|---|
| [생물 임용 노트] 효소 - 1) 효소의 개요 (0) | 2023.01.02 |
| [생물 임용 노트] 단백질 - 3) 단백질의 기능: 단백질의 기능, 리간드의 상호작용 (0) | 2022.12.29 |
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 분해 (0) | 2022.12.28 |
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 접힘 (0) | 2022.12.27 |


