| 일 | 월 | 화 | 수 | 목 | 금 | 토 |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | |||
| 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 |
| 26 | 27 | 28 | 29 | 30 | 31 |
- 글라이옥시좀
- 노션 단축키
- 네른스트 방정식
- 티스토리챌린지
- 광계
- 밀착연접
- 간극연접
- 차등 전위
- 인지질
- 캘빈회로
- 노션 필수 단축키
- 후구동물
- 퍼옥시좀
- 베타 산화
- 인슐린
- 오블완
- 노션 블록
- 수동수송
- 광호흡
- 전자전달 복합체
- 선구동물
- 초나선
- 신호서열
- 인테그린
- 역수송체
- 당지질
- 루비스코
- 당분해
- 콜레스테롤
- 단백질 분류
- Today
- Total
숭늉의 연구일지
[생물 임용 노트] 단백질 - 1) 아미노산: 정의, 종류, 양쪽성 이온 성질 본문
아미노산(amino acid)
단백질의 기본 구성단위로서 한 분자 안에 염기로 작용하는 아미노기(-NH2)와 산으로 작용하는 카르복시기(-COOH)를 모두 가진 양성적 성질의 유기 화합물을 총칭한다.

아미노산의 구조
1) α탄소를 갖는다 - 4개의 서로 다른 원자단을 가지며 거울상 이성질체가 존재한다.
2) 세포질 단백질은 모두 L형 아미노산을 이용한다.
3) R기의 구성에 따라 화학적 특성이 달라진다.
아미노산의 종류
아미노산은 R기의 성질에 따라 비극성, 방향족, 극성, 양전하, 음전하로 나뉜다.
검은색(정식 명칭), 빨간색(3글자 표기법)
1. 비극성 지방족(nonpolar, alipathic)
Group1: 소수성 상호작용을 통해 단백질 구조를 안정화
Group2: 가장 단순한 구조, 비극성이지만 소수성 상호작용을 하지 않음, 단백질의 유연한 구조를 형성
Group3: thioesther기를 가짐
Group4: 특이한 고리형 구조로 구조적 유연성을 감소시킴
→ 환상의 구조가 알파 탄소를 축으로 하는 회전에 제한을 받는다.
→ 단백질의 Loop나 Bending 지점에서 발견 됨

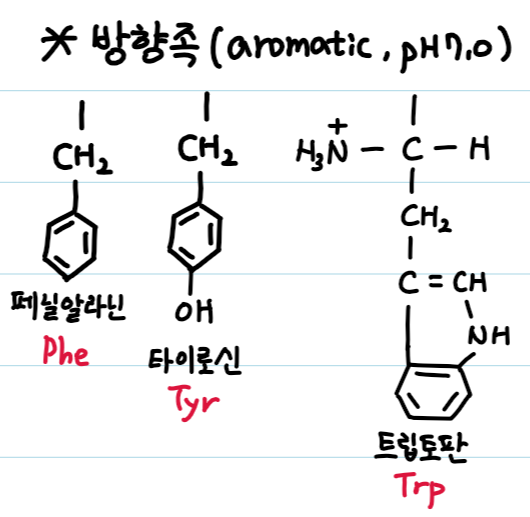
2. 방향족(aromatic, pH 7.0)
비교적 비극성으로 소수성 상호작용으로 관여가능
타이로신: -OH기는 극성으로 수소결합이 가능. 일부 효소의 기능기로 작용.
트립토판: 인돌 고리 질소 원자에 의해 극성을 갖는다. 고리구조를 가지므로 에너지 흡수와 방출을 일으킨다. 220nm에서 최대 흡광도를 갖는다.
3. 극성, 비전하(polar, uncharged, pH 7.0)
Group1: 친수성. -OH기는 인산화의 표적
Group2: -SH기에 의한 극성을 가짐. 2개의 시스테인이 이황결합체를 형성하여 시스틴(Cystine)을 형성한다.
Group3: -NH2기에 의한 극성을 갖는다. 산 또는 염기에 의해 가수분해 되어 아스파트산과 글루탐산을 만든다.

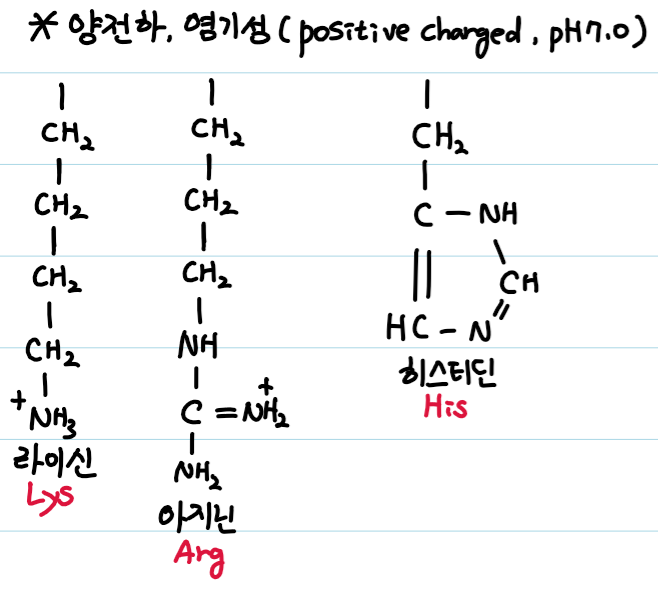
4. 양전하, 염기성(positive charged, pH7.0)
라이신: 아미노기를 갖는다.
아르지닌: 구아니디노기를 갖는다.
히스티딘: 이미다졸기를 갖는다. 중성의 pka에서 이온화가 가능한 곁사슬을 갖는다.

5. 음전하, 산성(negative charged, pH 7.0)
R기에 제 2의 카르복실기를 갖는다.
6. 비표준 아미노산
위에 제시된 20종의 아미노산은 표준 아미노산이며 잔기 변형으로 생겨난 비표준 아미노산 또한 존재한다.
<비표준 아미노산의 예>
1) 4-하이드록시 프롤린: 콜라겐에 존재
2) 5-하이드록시 리신: 콜라겐에 존재
3) 6-N-메틸 리신: 마이오신(myosin)에 존재
4) γ-카르복시 글루탐산: 트롬민, Ca2+ 결합 단백질에 존재
5) 데스모신(desmosin): 4 분자의 리신 잔기를 가짐. elastin에 존재한다.
6) 셀레노시스테인: 시스테인 황 대신 셀레늄 존재. 세린 유도체
7) 오르니틴, 시트룰린: 단백질에 없는 아미노산인 Arg(아르지닌) 생합성 및 요소회로의 중간체
아미노산의 양쪽성 이온(zwitter ion) 성질
아미노산은 양쪽성 이온으로 산 또는 염기로 작용한다. 즉 pH에 따라 H+를 흡수 또는 방출한다.

이에 따라 pk 값을 2개 가지게 되고 아미노산마다 다른 이온화 및 적정 곡선을 갖게 된다.

**pI(등전점): 알짜전하가 0인 완전한 양극성 상태
'생물학 임용노트 > 단백질' 카테고리의 다른 글
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 접힘 (0) | 2022.12.27 |
|---|---|
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 변성 (1) | 2022.12.26 |
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 3,4차 구조 (0) | 2022.04.21 |
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 단백질의 2차 구조 (0) | 2022.04.21 |
| [생물 임용 노트] 단백질 - 2) 단백질의 구조: 펩타이드, 1차~4차구조 개관, 일반적 특징 (0) | 2022.04.19 |


